センター試験の化学Ⅰの演習問題を紹介しています。このページは,窒素の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 窒素 |
|---|---|
| 年度 | 2014年度 |
| 問題番号 | 化学Ⅰ-第3問-問3 |
| 配点 | 3 |
| 計算問題 | × |
| 難易度 | 普通 |
正解
③ アンモニアを実験室で得るには,塩化アンモニウムに強酸を加える。
スポンサーリンク
解説
① 空気を構成する成分気体は窒素,酸素などですが,これらの沸点は異なります。空気を冷却すると液体になり,その液体空気の温度を少しずつ上げていくと,-196℃で窒素が気体になります。次いで,-183℃で酸素が気体になります。はじめに出てくる気体には窒素が多く含まれていますので,この操作を繰り返すことにより,窒素を分離して得ることができます。
② オストワルト法では,アンモニアNH3を酸化して一酸化窒素NOとし,これを空気酸化して二酸化窒素NO2を得て,さらに水H2Oと反応させることで硝酸HNO3を製造します。
4NH3 + 5O2 → 4NO + 6H2O
2NO + O2 → 2NO2
3NO2 + H2O → 2HNO3 + NO
③ 塩化アンモニウムは弱塩基の塩です。水酸化カルシウムなどの強塩基を加えることで,弱塩基の遊離によりアンモニアを得ることができます。強酸を加えても遊離は起こりません。
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O
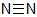
④ 窒素の原子価は3なので,1つの窒素原子から3本の共有結合を形成することができます。窒素N2では,互いに3本の共有結合を形成して右図のように三重結合をつくっています。
⑤ p-ヒドロキシアゾベンゼンに代表される芳香族アゾ化合物は,アゾ基を含んでいます。アゾ基は,「 -N=N- 」の構造をしており,窒素原子間の二重結合を含んでいます。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |