センター試験の化学の演習問題を紹介しています。このページは,純度の解説です。
高校化学Net参考書 ~センター試験演習「化学」~
問題情報
| 年度 | 2016年度 |
|---|---|
| 試験 | 本試験-化学 |
| 問題 | 第3問-問6 |
| 単元 | 純度 |
| 配点 | 4点 |
| 計算問題 | ○ |
| 難易度 | 難しい |
正解
⑤ 93
スポンサーリンク
解説
1molのFeK(SO4)2・12H2Oには,2molの硫酸イオンSO42-が含まれています。そのため,ここから生じる硫酸バリウムBaSO4は2molです。
これを質量〔g〕で考えると,FeK(SO4)2・12H2O=503,BaSO4=233より,
503g/mol×1mol : 233g/mol×2mol = 503g : 466g
よって,4.66gの沈殿が生じたことから,5.03gのFeK(SO4)2・12H2Oが含まれていたことになります。
全体の5.40gのうち,5.03gのFeK(SO4)2・12H2Oが含まれていたので,その純度は次のように求めることができます。
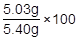 = 93.1% = 93%
= 93.1% = 93%
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |