センター試験の化学の演習問題を紹介しています。このページは,反応速度の問題です。
高校化学Net参考書 ~センター試験演習「化学」~
問題情報
| 年度 | 2017年度 |
|---|---|
| 試験 | 本試験-化学 |
| 問題 | 第2問-問3 |
| 単元 | 反応速度 |
| 配点 | a 3点 b 2点 |
| 計算問題 | ○ |
| 難易度 | 難しい |
問題
| 必要があれば,原子量および定数は次の値を使うこと。 H 1.0 C 12 N 14 O 16 S 32 Cl 35.5 Mn 55 Cu 64 Zn 65 実在気体とことわりがない限り,気体は理想気体として扱うものとする。 |
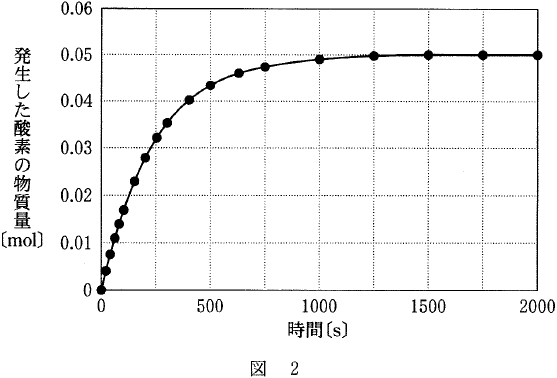
ある濃度の過酸化水素水100 mLに,触媒としてある濃度の塩化鉄(Ⅲ)水溶液を加え200 mLとした。発生した酸素の物質量を,時間を追って測定したところ,反応初期と反応全体では,それぞれ,図1と図2のようになり,過酸化水素は完全に分解した。この結果に関する下の問い(a・b)に答えよ。ただし,混合水溶液の温度と体積は一定に保たれており,発生した酸素は水に溶けないものとする。
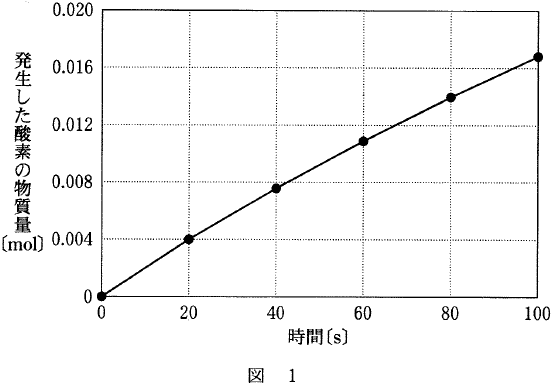
a 混合する前の過酸化水素水の濃度は何mol/Lか。最も適当な数値を,次の①~⑥のうちから一つ選べ。
① 0.050 ② 0.10 ③ 0.20 ④ 0.50 ⑤ 1.0 ⑥ 2.0
| ⑤ 1.0 【2H2O2 → O2 + 2H2O より,発生した酸素の2倍の過酸化水素が含まれていたことがわかります。図2より,0.050 molの酸素が発生しているので,過酸化水素は0.10 mol含まれていたことがわかります。過酸化水素水の体積が0.10 Lなので,1.0 mol/Lです。】 |
b 最初の20秒間において,混合水溶液中の過酸化水素の平均の分解速度は何mol/(L・s)か。最も適当な数値を,次の①~⑥のうちから一つ選べ。
① 4.0×10-4 ② 1.0×10-3 ③ 2.0×10-3
④ 4.0×10-3 ⑤ 1.0×10-2 ⑥ 2.0×10-2
| ③ 2.0×10-3 【塩化鉄(Ⅲ)水溶液の混合により体積が2倍になっているので,反応開始時の過酸化水素のモル濃度は0.50 mol/Lです。 図1より,最初の20秒間で0.0040 molの酸素が発生しており,0.0080 molの過酸化水素が反応したことがわかります。体積が0.20 Lなので,濃度の減少は0.040 mol/Lです。 20秒間で0.040 mol/Lの過酸化水素が分解したので,分解速度は0.0020 mol/(L・s)です。】 |
スポンサーリンク
| ワードファイル |  |
|---|