センター試験の化学Ⅰの演習問題を紹介しています。このページは,反応熱の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 反応熱 |
|---|---|
| 年度 | 2007年度 |
| 問題番号 | 化学Ⅰ-第2問-問1 |
| 配点 | 4 |
| 計算問題 | × |
| 難易度 | 難しい |
正解
③ COの燃焼熱の値は正である。したがって,COの生成熱はCO2の生成熱よりも大きい。
スポンサーリンク
解説
① 蒸発熱は必ず吸熱反応なので,絶対値で表されます。凝縮するときには逆に発熱反応となります。蒸発熱の他に,融解熱や結合エネルギーも必ず吸熱反応なので,蒸発熱と同様に絶対値で表されます。
② Mgの燃焼熱と,MgOの生成熱は,同じ熱化学方程式で表されます。
Mg + 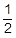 O2 = MgO + 602kJ
O2 = MgO + 602kJ
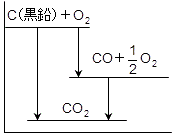 ③ 記述の内容をエネルギー図で表すと,右図のようになります。発熱反応だと下へ向かいます。COの燃焼熱が正の値なので,CO2は下に位置します。このとき,C(黒鉛)+O2から下へ向かう幅は,CO2の方が大きくなります。つまり,COの生成熱よりもCO2の生成熱の方が大きいということです。よって,③の記述は誤りです。
③ 記述の内容をエネルギー図で表すと,右図のようになります。発熱反応だと下へ向かいます。COの燃焼熱が正の値なので,CO2は下に位置します。このとき,C(黒鉛)+O2から下へ向かう幅は,CO2の方が大きくなります。つまり,COの生成熱よりもCO2の生成熱の方が大きいということです。よって,③の記述は誤りです。
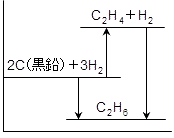 ④ 記述の内容をエネルギー図で表すと,右図のようになります。エチレンにH2が付加してエタンが生成する反応が下向きなので,この反応は発熱反応です。
④ 記述の内容をエネルギー図で表すと,右図のようになります。エチレンにH2が付加してエタンが生成する反応が下向きなので,この反応は発熱反応です。
⑤ 反応熱が正の値なので,熱が発生します。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |