センター試験の化学Ⅰの演習問題を紹介しています。このページは,燃焼の量的関係の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 燃焼の量的関係 |
|---|---|
| 年度 | 2007年度 |
| 問題番号 | 化学Ⅰ-第4問-問7 |
| 配点 | 4 |
| 計算問題 | ○ |
| 難易度 | 難しい |
正解
② 0.006
スポンサーリンク
解説
まず,nの値を求めるために,「ケトン全体の質量」に対する「水素原子の質量」で方程式をつくります。
分子量で考えると,ケトンCnHn+4Oの分子量は,
12×n + 1.0×(n+4) + 16×1 = 13n + 20
です。また,水素原子だけの相対質量は,1.0×(n+4)です。
一方,具体的な質量の値が与えられています。ケトンの質量は98mgです。また,生じた水から水素原子の質量を求めると,
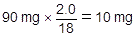
となります。
よって,「ケトン全体の質量」に対する「水素原子の質量」で方程式をつくると次のようにnを求めることが出来ます。
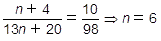
次に,水の質量から水の物質量〔mol〕を求めます。
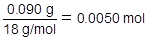
ケトンの完全燃焼を化学反応式で表すと,次のようになります。
4CnHn+4O + (5n+2)O2 → 4nCO2 + 2(n+4)H2O
ここにn=6を代入して整理すると,次のように表すことが出来ます。
C6H10O + 8O2 → 6CO2 + 5H2O
化学反応式の係数の比は物質量の比なので,次のようにして二酸化炭素の物質量xを求めることが出来ます。
6:5 = x:0.0050 ⇒ x=0.0060
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |