センター試験の化学Ⅰの演習問題を紹介しています。このページは,窒素酸化物の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 窒素酸化物 |
|---|---|
| 年度 | 2010年度 |
| 問題番号 | 化学Ⅰ-第3問-問1 |
| 配点 | 3 |
| 計算問題 | × |
| 難易度 | 易しい |
正解
① 一酸化窒素は,銅に濃硝酸を反応させて得られる。
スポンサーリンク
解説
① 硝酸は強い酸化剤ですが,濃度によって変化後に生じる物質が違います。濃硝酸なら二酸化窒素NO2を生じ,希硝酸なら一酸化窒素NOを生じます。
濃硝酸:HNO3 + H+ + e- → NO2 + H2O
希硝酸:HNO3 + 3H+ + 3e- → NO + 2H2O
② 一酸化窒素NOは,水に溶けにくい気体です。一方,二酸化窒素NO2は水に溶けやすい気体なので,注意しましょう。
③ 一酸化窒素NOは,酸素に触れるだけで容易に二酸化窒素NO2になります。このとき無色から赤褐色へと変化します。
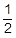 NO + O2 →
NO + O2 → 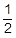 NO2
NO2
④ 二酸化窒素NO2は,赤褐色の気体です。
⑤ 酸性酸化物に分類される二酸化窒素NO2は,水H2Oと反応して,オキソ酸である硝酸HNO3を生じます。このとき,一酸化窒素NOが副生成物として生じることに注意が必要です。
2NO2 + H2O → 2HNO2 + NO
⑥ 二酸化窒素NO2は,四酸化二窒素N2O4と平衡状態にあります。低温にすると無色の四酸化二窒素の割合が大きくなり,赤褐色がうすくなります。
2NO2 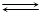 N2O4
N2O4
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |