センター試験の化学Ⅰの演習問題を紹介しています。このページは,沈殿の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 沈殿 |
|---|---|
| 年度 | 2010年度 |
| 問題番号 | 化学Ⅰ-第3問-問2 |
| 配点 | 4 |
| 計算問題 | × |
| 難易度 | 易しい |
正解
③
スポンサーリンク
解説
アルカリ金属やアルカリ土類金属を除くほとんどの金属イオンは,水酸化物イオンOH-による沈殿を生じます。水酸化ナトリウムNaOH水溶液は,もちろん水酸化物イオンOH-が含まれています。アンモニアNH3水も,水と反応することで水酸化物イオンOH-を生じています。
NH3 + H2O 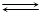 NH4+ + OH-
NH4+ + OH-
しかし,錯イオンを生じる条件になれば,その沈殿は溶けます。両性元素であるAl,Zn,Sn,Pb(あ あ すん なり)のイオンは,強塩基である水酸化ナトリウム水溶液を過剰に加えることで錯イオンとなります。また,アンモニア分子NH3と錯イオンをつくる金属もあり,Ag,Cu,Znの3つを覚えておく必要があります。
① Zn2+ + 2OH- → Zn(OH)2
Zn(OH)2 + 2OH- → [Zn(OH)4]2-
② Pb2+ + 2OH- → Pb(OH)2
Pb(OH)2 + 2OH- → [Pb(OH)4]2-
③ Al3+ + 3OH- → Al(OH)3
アンモニア水は弱い塩基性なので,過剰に加えても錯イオン[Al(OH)4]-は生じません。また,アルミニウムAlは,アンモニア分子NH3と錯イオンを形成する金属ではありません。
④ Cu2+ + 2OH- → Cu(OH)2
Cu(OH)2 + 4NH3 → [Cu(NH3)4]2+ + 2OH-
⑤ 2Ag+ + 2OH- → Ag2O + H2O
Ag2O + 4NH3 + H2O → 2[Ag(NH3)2]+ + 2OH-
銀イオンAg+と水酸化物イオンOH-の反応で生じると考えられる水酸化銀AgOHは非常に不安定で,すぐに分解して酸化銀Ag2Oの褐色沈殿を生じます。AgOHが得られない以上,Ag2Oが生成する化学反応式を書かなければいけませんので,注意が必要です。
ちなみに,水酸化銅(Ⅱ)Cu(OH)2も比較的不安定で,加熱すると容易に分解します。
Cu(OH)2 → CuO + H2O
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |