センター試験の化学Ⅰの演習問題を紹介しています。このページは,ハロゲン,金属の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | ハロゲン,金属 |
|---|---|
| 年度 | 2010年度 |
| 問題番号 | 化学Ⅰ-第3問-問3 |
| 配点 | a‐3,b‐3 |
| 計算問題 | × |
| 難易度 | 普通 |
正解
④ 臭素を塩化カリウム水溶液に加えると,塩素が生成する。
③ カルシウムは水と反応し,酸素が発生する。
スポンサーリンク
解説
a ① フッ素は酸素よりも陰性の強い元素です。そのため,水H2O中の酸素原子(酸化数-2)が単体O2(酸化数0)になり,フッ素F2(酸化数0)がフッ化水素HF(酸化数-1)になります。
2H2O + 2F2 → 4HF + O2
② 塩素Cl2は水H2Oと反応して,塩化水素HClと次亜塩素酸HClOを生じます。次亜塩素酸は強い酸化作用をもつため殺菌や漂白に用いられます。
Cl2 + H2O 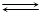 HCl + HClO
HCl + HClO
③ 臭素は,常温で赤褐色の液体です。全元素中で,常温常圧で単体が液体なのは水銀Hgと臭素Br2だけです。非金属元素では臭素Br2だけ,金属元素では水銀Hgだけです。
④ 臭素と塩素では,塩素の方が陰性の強い元素です。そのため,塩素の方が酸化数-1となりやすい関係にあります。臭素Br2では塩化カリウムKCl(酸化数-1)を単体の塩素Cl2(酸化数0)にすることは出来ません。
⑤ ヨウ素I2は水に溶けにくい物質ですが,ヨウ化カリウムKI水溶液には溶けます。これは,ヨウ素I2とヨウ化物イオンI-が反応して三ヨウ化物イオンI3-というイオンを生じるためです。
I2 + I- → I3-
⑥ ヨウ素は常温で黒紫色の固体です。昇華性の物質で,固体と気体の状態変化をします。
b ① マグネシウムは冷水とはほとんど反応しません。ただ,温度を上げると反応することが出来ます。この他にも,アルカリ土類金属と異なる性質が多いため,マグネシウムMgはアルカリ土類金属に含まれません。
Mg + 2H2O → Mg(OH)2 + H2
② アルミニウムは不動態をつくる金属です。表面に緻密な酸化被膜を生じると,その内部にまで酸素O2や塩酸HClなどが入れないので,反応しにくい状態になります。この状態を不動態といいます。クロムCr,鉄Fe,コバルトCo,ニッケルNi,アルミニウムAlなどが不動態をつくる金属で,「黒柳徹子にある不動態」と覚えましょう。
③ カルシウムなどの陽性の強い金属は,水分子H2O中の水素原子1個と置き換わって,酸化数がプラスの状態になります。このときに水素は酸化数0の単体H2になります。酸素O2が発生するというのは誤りです。
④ スズは両性元素なので,強塩基の水溶液と反応して錯イオンを形成し,溶けます。アルミニウムAl,亜鉛Zn,スズSn,鉛Pbが代表的な両性元素で,「あ あ すん なり」と覚えましょう。
⑤ 銀は,最も電気伝導性の高い金属です。熱伝導性も最も高い値を示します。
⑥ 水銀は多くの金属との合金をつくります。それらを総称してアマルガムと呼んでいます。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |