センター試験の化学Ⅰの演習問題を紹介しています。このページは,硫化物の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 硫化物 |
|---|---|
| 年度 | 2010年度 |
| 問題番号 | 化学Ⅰ-第3問-問4 |
| 配点 | 4 |
| 計算問題 | ○ |
| 難易度 | 難しい |
正解
⑤ 94
スポンサーリンク
解説
まず,中性水溶液で硫化水素H2Sを通じたときに沈殿する金属を確認します。硫化水素を通じたときに沈殿を生じるかどうかは,イオン化列を基にグループ分けすることが出来ます。
~Al 液性に関係なく,沈殿しない。
Zn~Ni 中性・塩基性の場合,沈殿する。
Sn~ 液性に関係なく,沈殿する。
よって,硫化マグネシウムMgSは沈殿せず,硫化亜鉛ZnSの沈澱が生じます。
次に,沈殿の質量から,そこに含まれる亜鉛の質量を求めます。ZnS=65+32=97,Zn=65 なので,ZnSが97gあれば,Znが65g含まれていることになります。今は0.097gの硫化亜鉛があるので,そこに含まれる亜鉛は0.065gです。
97g : 65g = 0.097g : x
x = 0.065g
合金が1.000gあるうちの0.065gが亜鉛なので,残りの0.935gがマグネシウムの質量です。その割合は,
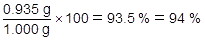
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |