センター試験の化学Ⅰの演習問題を紹介しています。このページは,身のまわりの化学の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 身のまわりの化学 |
|---|---|
| 年度 | 2011年度 |
| 問題番号 | 化学Ⅰ-第1問-問6 |
| 配点 | 4 |
| 計算問題 | × |
| 難易度 | 易しい |
正解
⑤ 塩素水に含まれている次亜塩素酸は還元力が強いので,塩素水は殺菌剤として使われている。
スポンサーリンク
解説
① ナトリウムNaは,炎色反応で黄色を呈します。代表的な炎色反応は覚えておきましょう。
リアカー 無き K村, 動力 借ろうと するもくれない 馬力。
Li赤 Na黄 K紫 Cu緑 Ca橙 Sr紅 Ba緑
② ジュラルミンは,アルミニウムAlの他に銅Cu,マグネシウムMg,マンガンMnなどを含んでいます。軽くて強度が大きいため,航空機材料に用いられています。
③ ガラスは二酸化ケイ素SiO2を主成分として炭酸ナトリウムNa2CO3などを原料に製造されています。その工業的製法であるアンモニアソーダ法(ソルベー法)は,次の5つの反応からなっています。
・溶解度の低い炭酸水素ナトリウムNaHCO3を沈殿させる。
NaCl + H2O + NH3 + CO2 → NaHCO3 + NH4Cl
・炭酸水素ナトリウムを熱分解して,炭酸ナトリウムを得る。
2NaHCO3 → Na2CO3 + H2O + CO2
・炭酸カルシウムCaCO3を熱分解して,原料の二酸化炭素CO2をつくる。
CaCO3 → CaO + CO2
・アンモニアNH3を遊離するための強塩基をつくる。
CaO + H2O → Ca(OH)2
・弱塩基の遊離により,原料のアンモニアをつくる。
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O
上記の5つの式を1つにまとめると,次の式で表されます。
2NaCl + CaCO3 → Na2CO3 + CaCl2
④ ヨウ素I2には昇華性があります。そのため,気体のヨウ素を冷却すると,液体にならずに固体になります。ヨウ素の他,二酸化炭素(ドライアイス)やナフタレン,p‐ジクロロベンゼンも昇華性の物質です。
⑤ 塩素Cl2は,水H2Oと次のように反応して塩酸HClと次亜塩素酸HClOを生じます。
Cl2 + H2O 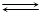 HCl + HClO
HCl + HClO
次亜塩素酸は「酸化力」が強く,殺菌や漂白に利用されています。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |