センター試験の化学Ⅰの演習問題を紹介しています。このページは,同素体,電子数の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 同素体,電子数 |
|---|---|
| 年度 | 2013年度 |
| 問題番号 | 化学Ⅰ-第1問-問1 |
| 配点 | 1-3,b-3 |
| 計算問題 | × |
| 難易度 | 易しい |
正解
a ⑥ 黄リンと赤リン
b ④ メタン
スポンサーリンク
解説
a 「同じ元素からできている単体で性質の異なる物質」を互いに同素体といいます。一番のポイントは「単体」だということです。③,④,⑤は複数の種類の元素からなる「化合物」なので同素体の組合せではありません。この他,一酸化炭素COと二酸化炭素CO2,水H2Oと過酸化水素H2O
また,①は同族元素(希ガス),②は同位体です。同素体と同位体は特に間違えて覚えやすいので,しっかりと区別しておきましょう。
高校の化学で登場する同素体は,
・硫黄Sの同素体(斜方硫黄S8,単斜硫黄S8,ゴム状硫黄Sx)
・炭素Cの同素体(黒鉛C,ダイヤモンドC,フラーレンC60など)
・酸素Oの同素体(酸素O2,オゾンO3)
・リンPの同素体(黄リンP4,赤リンPx)
の4種類です。「スコップ(SCOP)どうぞ」と覚えましょう。「どうぞ」の部分は同素体を表し,同位体との覚え間違いを防ぐために付けました。
b 単なる電子の総数ではなく,「結合に使われている」電子の総数だということを読み飛ばしてしまわないように気を付けましょう
選択肢の物質はすべて非金属元素でできているので,共有結合で分子をつくっています。単結合1か所につき1対(2個)の電子,二重結合1か所につき2対(4個)の電子,三重結合1か所につき3対(6個)の電子が結合に使われています。
それぞれの物質を構造式で表すと次のようになります。ちなみに,物質名のあとの数字は,結合に使われている電子の総数です。
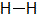 ① 水素(2) | 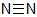 ② 窒素(6) | 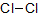 ③ 塩素(2) |
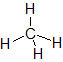 ④ メタン(8) | 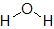 ⑤ 水(4) | 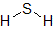 ⑥ 硫化水素(4) |
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |