センター試験の化学Ⅰの演習問題を紹介しています。このページは,原子の数の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 原子の数 |
|---|---|
| 年度 | 2013年度 |
| 問題番号 | 化学Ⅰ-第1問-問4 |
| 配点 | 4 |
| 計算問題 | ○ |
| 難易度 | 普通 |
正解
① 標準状態のアンモニア22.4Lに含まれる水素原子の数
スポンサーリンク
解説
すべての選択肢で「数」を求める問題ですが,大小関係を比較するだけなので,面倒な計算は省略すべきです。物質量(mol),質量(g),標準状態の気体の体積(L),数(個)は,すべて比例の関係にあります。つまり,物質量(mol)を比較したときに大きい方は,数(個)を比較したときも大きいのです。ここでは,物質量(mol)を求めて,その値が最も大きいものが数(個)も多いと判断します。
① 標準状態の気体は,1molで22.4Lです。よって,標準状態で22.4LのアンモニアNH3は1molです。
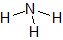
ただし,問われているのは,アンモニア分子の数ではなく,水素原子の数だということに注意しましょう。アンモニア分子1個には,水素原子3個が含まれています。アンモニア分子が2個あれば,水素原子は6個あります。ここから,アンモニア分子の数とそこに含まれる水素原子の数は1:3の比だということが分かります。よって,アンモニア分子が1molあることから,水素原子は3molと求めることができます。
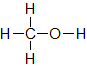
② メタノールCH3OH分子1個には,酸素原子1個が含まれています。メタノール分子が2個あれば,酸素原子は2個あります。ここから,メタノールの数とそこに含まれる酸素原子の数は1:1だということが分かります。よって,メタノール1molに含まれる酸素原子は1molです。
③ ヘリウムは希ガスなので,単原子分子として存在しています。そのため,ヘリウム1molはヘリウム原子1molのことです(二原子分子である水素H2が1molあれば,水素原子Hは2molになる)。
また,ヘリウムは原子番号2なので,ヘリウム原子1個の中に陽子が2個存在しています。原子の状態では陽子数と電子数は等しい(電気的に中性)ので,ヘリウム原子1個の中に電子が2個含まれていることになります。ヘリウム原子が2個あれば,電子は4個あります。ここから,ヘリウム原子の数とそこに含まれる電子の数は1:2だということが分かります。よって,ヘリウム1molに含まれる電子は2molです。
④ 1mol/Lの塩化カルシウム水溶液1L中には,1mol/L × 1L = 1mol の塩化カルシウムCaCl2が含まれています。また,塩化カルシウムは金属元素(Ca)と非金属元素(Cl)でできている化合物なので,イオン結晶として存在しています。水に溶かして電離した時のイオン反応式「CaCl2 → Ca2+ + 2Cl-」の係数比からも分かるように,1molのCaCl2には2molの塩化物イオンCl-が含まれています。
⑤ 黒鉛(グラファイト)は組成式Cで表され,その式量は12です。よって,
12g ÷ 12g/mol = 1mol の炭素原子が含まれています。
物質量を比較すると,①が3molで最も大きいことが分かります。よって,数で考えても①が最も多いと判断することができます。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |