センター試験の化学Ⅰの演習問題を紹介しています。このページは,工業的製法の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 工業的製法 |
|---|---|
| 年度 | 2013年度 |
| 問題番号 | 化学Ⅰ-第3問-問1 |
| 配点 | 4 |
| 計算問題 | × |
| 難易度 | 普通 |
正解
④ フッ化水素は,蛍石(フッ化カルシウム)に濃塩酸を加え,加熱して製造される。
スポンサーリンク
解説
① 銑鉄は,約4.0%の炭素や微量のケイ素,リン,硫黄などを含んだ鉄です。かたくてもろい性質というがあります。高温の銑鉄に酸素を吹き込むと,炭素などが酸化されて取り除かれます。こうしてできた鉄は炭素を約0.02~2.0%含む鋼になります。鋼はかたくて強いという性質があります。
② アンモニアNH3は,鉄を主成分とする触媒を用いて水素H2と窒素N2を反応させることでつくられます。この工業的製法をハーバー・ボッシュ法(またはハーバー法)といいます。
N2 + 3H2 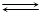 2NH3
2NH3
③ 硝酸は,オストワルト法(またはオストワルド法)により合成されます。アンモニアNH3を白金触媒を用いて酸化し,一酸化窒素NOとします。一酸化窒素NOを空気酸化して二酸化窒素NO2を得ます。さらに,二酸化窒素NO2を水H2Oと反応させて硝酸HNO3を合成します。
4NH3 + 5O2 → 4NO + 6H2O
2NO + O2 → 2NO2
3NO2 + H2O → 2HNO3 + NO
最後の式を書き出すとき,一酸化窒素が副生することを知らなければ化学反応式を完成させることができません。このときに副生する一酸化窒素NOは,前の反応の原料として用いられます。
④ フッ化水素HFは,弱酸の遊離を利用して合成されます。弱酸の塩であるフッ化カルシウムCaF2に強酸を加えることで,弱酸のフッ化水素HFが遊離されます。
CaF2 + H2SO4 → CaSO4 + 2HF
強酸なら濃塩酸でもいいかというと,少し問題があります。塩酸からは溶質の塩化水素HClが出てきてしまい,不純物として混ざります。そのため,不揮発性の硫酸を用いるのです。
⑤ 空気はいろんな気体の混合物ですが,成分気体はそれぞれ沸点が異なります。空気の大半を占める窒素の沸点は-196℃,酸素の沸点は-183℃です。この温度よりも冷却すると,どちらも液体になります。ここから徐々に温度を上げると,沸点の低い窒素が気体になります。その後,さらに温度を上げると純粋な酸素の気体を得ることができます。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |