センター試験の化学基礎の演習問題を紹介しています。このページは,量的関係の解説です。
高校化学Net参考書 ~センター試験演習「化学基礎」~
問題情報
| 年度 | 2016年度 |
|---|---|
| 試験 | 本試験-化学基礎 |
| 問題 | 第2問-問2 |
| 単元 | 量的関係 |
| 配点 | 4点 |
| 計算問題 | ○ |
| 難易度 | 難しい |
正解
② CH3OH
スポンサーリンク
解説
この問題は,「化学」の有機化合物の分野でよく見られるものです。「化学基礎」しか学習していない生徒には難しいかもしれません。
選択肢から,この有機化合物を構成する元素は,C,H,Oのみと考えられます。ただし,Oは含まれていない可能性もあります。
そこで,この有機化合物の組成式をCxHyOzとおくと,その完全燃焼は次の反応式で表されます。
CxHyOz + aO2 → xCO2 + 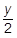 H2O
H2O
生じた二酸化炭素に含まれる炭素原子は,有機化合物に含まれていたものです。同様に,生じた水に含まれる水素原子も有機化合物に含まれていたものです。一方,酸素原子は,有機化合物に含まれていたものなのか,燃焼するときに反応した酸素O2のものなのか判断できません。
反応式から,二酸化炭素の物質量〔mol〕と有機化合物に含まれる炭素原子の物質量〔mol〕が等しいことがわかります。
CO2=44より, =0.025mol
=0.025mol
同様に,水の物質量〔mol〕を2倍すると有機化合物に含まれる水素原子の物質量〔mol〕と等しくなります。
H2O=18より,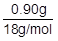 ×2=0.10mol
×2=0.10mol
ここで,炭素原子0.025molと水素原子0.10molの質量の総和を求めると,
12g/mol×0.025mol + 1.0g/mol×0.10mol = 0.30g + 0.10g = 0.40g です。
また,有機化合物は0.80gあったわけですから,残りの0.40gが酸素原子だとわかります。
O=16より, =0.025mol
=0.025mol
有機化合物に含まれる炭素原子,水素原子,酸素原子の物質量の最も簡単な整数比は,0.025mol:0.10mol:0.025mol = 1:4:1 です。よって,組成式はCH4Oです。
この組成式に当てはまる選択肢である②CH3OHが正解です。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |