センター試験の化学Ⅰの演習問題を紹介しています。このページは,熱化学の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 熱化学 |
|---|---|
| 年度 | 2009年度 |
| 問題番号 | 化学Ⅰ-第2問-問2 |
| 配点 | 4 |
| 計算問題 | ○ |
| 難易度 | 難しい |
正解
① 黒鉛<ダイヤモンド<フラーレンC60
スポンサーリンク
解説
同じ質量〔g〕で考えるという条件ですが,同じ物質量〔mol〕で考えても同じ大小関係になります。ここでは,60molの炭素原子Cで考えることにします。すると,それぞれの熱化学方程式は次のように表されます。
60C(ダイヤモンド) + 60O2(気) = 60CO2(気) + 23760kJ・・・(1)
C60(フラーレン) + 60O2(気) = 60CO2(気) + 25930kJ・・・(2)
60C(黒鉛) = 60C(ダイヤモンド) - 120kJ・・・(3)
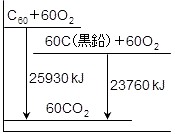 まず,ダイヤモンドとフラーレンの化学エネルギーを比較します。(1),(2)より,同じ物質になるときに,フラーレンからの方が多くの熱量を発生しています。これは,元々の化学エネルギーが,黒鉛よりも大きいからです。
まず,ダイヤモンドとフラーレンの化学エネルギーを比較します。(1),(2)より,同じ物質になるときに,フラーレンからの方が多くの熱量を発生しています。これは,元々の化学エネルギーが,黒鉛よりも大きいからです。
よって, ダイヤモンド<フラーレンC60 となります。
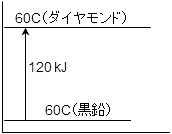 次に,(3)式より黒鉛とダイヤモンドの化学エネルギーを比較します。ダイヤモンドの化学エネルギーから熱量を引いた値が黒鉛の化学エネルギーと等しくなっています。つまり,ダイヤモンドの化学エネルギーの方が大きいということです。
次に,(3)式より黒鉛とダイヤモンドの化学エネルギーを比較します。ダイヤモンドの化学エネルギーから熱量を引いた値が黒鉛の化学エネルギーと等しくなっています。つまり,ダイヤモンドの化学エネルギーの方が大きいということです。
よって, 黒鉛<ダイヤモンド となります。
これらをまとめると, 黒鉛<ダイヤモンド<フラーレンC60 の関係を導くことが出来ます。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |