センター試験の化学Ⅰの演習問題を紹介しています。このページは,分子の数,原子を構成する粒子の数の解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 分子の数,原子を構成する粒子の数 |
|---|---|
| 年度 | 2014年度 |
| 問題番号 | 化学Ⅰ-第1問-問1 |
| 配点 | a-3,b-3 |
| 計算問題 | ○ |
| 難易度 | 普通 |
正解
a ① 水
b ④ 3:4
スポンサーリンク
解説
a 分子の数は「物質量〔mol〕×アボガドロ定数〔/mol〕」で求めることができますが,今回のセンター試験ではアボガドロ定数は与えられていません。ただ,大小関係を比較するだけならば,物質量〔mol〕を比較することで可能です。
物質量〔mol〕は,質量をw,分子量をMとおくと,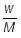 で求めることができます。
で求めることができます。
質量は1gで固定されていますので,分子量Mが小さい物質ほどその物質量〔mol〕が大きくなります。よって,分子量が最も小さい水H2Oの物質量〔mol〕が最も大きく,分子の数も最も多くなります。
b 炭素原子であれば,陽子の数は6個です。
また,「質量数=陽子の数+中性子の数」なので,質量数14の炭素原子は14-6=8より,中性子8個を含んでいます。
よって,陽子の数:中性子の数=6:8=3:4 です。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |