センター試験の化学Ⅰの演習問題を紹介しています。このページは,亜鉛とアルミニウムの解説です。
高校化学Net参考書 ~センター試験演習「化学Ⅰ」~
問題情報
| 単元 | 亜鉛とアルミニウム |
|---|---|
| 年度 | 2014年度 |
| 問題番号 | 化学Ⅰ-第3問-問4 |
| 配点 | 4 |
| 計算問題 | × |
| 難易度 | 普通 |
正解
④ 陽イオンを含む水溶液にアンモニア水を加えていくと,白い沈殿が生じるが,さらに加えるとその沈殿が溶ける。
スポンサーリンク
解説
① 金属の単体のうち,両性金属なら水酸化ナトリウム水溶液に溶けます。代表的な両性金属は,亜鉛Zn,アルミニウムAl,スズSn,鉛Pb(「ああすんなり」と覚える)です。よって,亜鉛とアルミニウムはどちらも水酸化ナトリウム水溶液に溶けます。
また,希塩酸に溶けるのは,例外を除き,イオン化傾向が水素Hよりも大きい金属です。亜鉛もアルミニウムもHよりイオン化傾向が大きいので,希塩酸に溶けます。
② 空気中で強熱したときに,酸化物が生成する金属は,イオン化傾向が銅Cuよりも大きいものです(銅は酸化されるが,水銀Hgは酸化されない)。亜鉛とアルミニウムはどちらも空気中で強熱すると,酸化物を生じます。
③ 高温の水蒸気と反応する金属は,イオン化傾向が鉄Feよりも大きいものです(鉄は反応するが,ニッケルは反応しない)。また,このとき水素H2が発生して金属の酸化物が生じます。よって,亜鉛とアルミニウムはどちらも高温の水蒸気と反応して,水素が発生します。
④ 陽イオンを含む水溶液にアンモニア水を加えていくと,通常は水酸化物の沈澱を生じます(NH3 + H2O 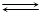 NH4+ + OH- により塩基性になっているため)。
NH4+ + OH- により塩基性になっているため)。
また,水酸化物の沈澱を生じたところにアンモニア水をさらに加えたとき,金属イオンがアンモニア分子NH3と錯イオンをつくる場合は,沈殿が溶けます。
アンモニア分子と錯イオンをつくる金属イオンは,銀イオンAg+,銅(Ⅱ)イオンCu2+,亜鉛イオンZn2+です。よって,陽イオンを含む水溶液にアンモニア水を加えていくと白い沈殿が生じ,さらに加えるとその沈殿が溶けるのは,亜鉛のみです。アルミニウムの場合は,白い沈殿が生じますが,その沈殿は溶けません。
スポンサーリンク
| 問題 | |
|---|---|
| ワードファイル |  |