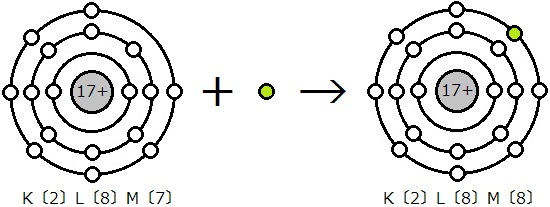「イオン」のページです。
高校化学Net参考書 ~化学基礎~
高校化学Net参考書 > 「化学基礎」 > 化学結合と結晶 > イオン
イオン
原子は陽子数=電子数なので電気的に中性(プラスマイナス0)ですが,数のバランスが崩れると電荷をもつようになります。このような,電荷をもつ粒子をイオンといいます。
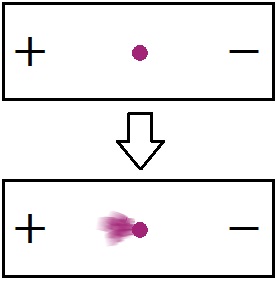
イオンの存在は,電圧をかけることによって確認することができます。例えば,湿らせたろ紙に,過マンガン酸カリウムKMnO4の粉末を置きます。このろ紙の両端に電圧をかけると,赤紫色が正極の方へと流れ始めます。このことから,負電荷をもつ赤紫色をした粒子(陰イオン)の存在が確認できます。
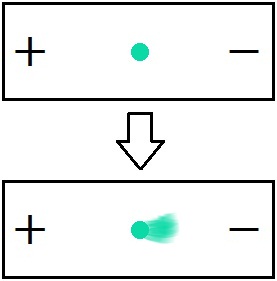
また,塩化銅(Ⅱ)CuCl2で同様の実験をすると,青色が負極の方へ移動します。このことから,正電荷をもつ青色をした粒子(陽イオン)の存在が確認できます。
イオンには様々な種類があり,無色のものも多く存在します。
スポンサーリンク
イオンの生成
希ガスの電子配置は非常に安定です。そのため,電荷のバランスを崩してでも希ガスと同じ電子配置をとろうとする原子がたくさんあります。
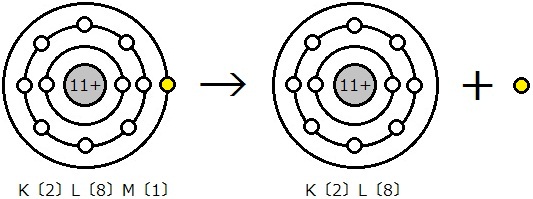
例えば,ナトリウム原子11Naは,K〔2〕L〔8〕M〔1〕という電子配置です。M殻の1個の電子を失うことで,ネオンNeと同じ電子配置K〔2〕L〔8〕になります。陽子数は11個のままで,電子数が10個になっていますので,プラスが1個多い状態です。このように,プラスが多くなってできるものを陽イオンといいます。
また,塩素原子17Clは,K〔2〕L〔8〕M〔7〕という電子配置です。M殻が1個の電子を受け取ることで,アルゴンArと同じ電子配置K〔2〕L〔8〕M〔8〕になります。陽子数は17個のままで,電子数が18個になっていますので,マイナスが1個多い状態です。このように,マイナスが多くなってできるものを陰イオンといいます。
ちなみに,ナトリウム原子Naが7個の電子を受け取ってアルゴンArと同じ電子配置になったり,塩素原子Clが7個の電子を放出してネオンNeと同じ電子配置になったりすることも考えられそうです。しかし,多くの電子の受け渡しは大きなエネルギーを必要とするので,通常は起こりません。
一般に,価電子数が1~3個の場合は電子を失って陽イオンになりやすく,価電子数が6,7個の場合は電子を受け取って陰イオンになりやすい傾向があります。価電子が4,5個の場合は,陽イオンにも陰イオンにもなりにくいことがわかっています。
スポンサーリンク