「分子量・式量」のページです。
高校化学Net参考書 ~化学基礎~
高校化学Net参考書 > 「化学基礎」 > 物質量と化学反応式 > 分子量・式量
分子量
質量数の異なる原子(同位体)が存在しているため,原子が共有結合でつながってできた「分子」にも異なる質量のものがあります。例えば,塩素原子には35Clと37Clがあります。そのため,塩素分子Cl2には
- 35Cl-35Cl
- 35Cl-37Cl
- 37Cl-37Cl
の3種類が存在しています(「37Cl-35Cl」は「35Cl-37Cl」と同じ分子です。分子を回転させると同じだということがわかります)。
元素の原子量を考えたときと同じように,天然存在比を考慮した平均値を求めることで,実験準備やデータ処理に用いる「分子の相対質量(分子量)」を求めることができます。ただ,分子を構成する原子の数が増えるほど,複雑になってしまいます。
そこで,通常は原子量の総和を求めて分子量とします。塩素の原子量35.5は,すべての塩素原子を均一化して相対質量を35.5と考えたものです。2個の塩素原子Clでできた塩素分子Cl2の分子量は35.5×2=71.0と考えることができます。分子量も原子量と同様に,単位がありません。
ちなみに,固体が分子結晶に分類される物質に対してのみ,分子量という言葉を使います。
スポンサーリンク
組成式で表される物質の式量
固体がイオン結晶,金属結晶,共有結合の結晶(共有結晶)に分類される物質は,構成粒子の数が決まっていないため,最も簡単な整数比である組成式で表します。
このような物質の相対質量を表すときには,組成式に書かれている原子について原子量の総和を求めます。このときの相対質量を式量といいます。
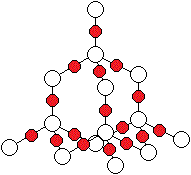 例えば,二酸化ケイ素SiO2は多数のケイ素原子Siと酸素原子Oがすべて共有結合で結びついている共有結合の結晶(共有結晶)です。組成式のSiO2に基づき,式量は28×1+16×2=60です(Si=28,O=16)。式量についても単位はありません。
例えば,二酸化ケイ素SiO2は多数のケイ素原子Siと酸素原子Oがすべて共有結合で結びついている共有結合の結晶(共有結晶)です。組成式のSiO2に基づき,式量は28×1+16×2=60です(Si=28,O=16)。式量についても単位はありません。
イオンの式量
イオンについても相対質量を考えることができます。このときの相対質量も式量といいます。
イオンは,電荷のバランスが崩れた状態です。これは,陽子に比べて電子が少なくなっている(陽イオン)のか,多くなっている(陰イオン)のかのどちらかです。
ここで思い出してほしいのが,陽子や中性子に比べて電子の質量は非常に小さい(1/1840)ということです。そのため,電子の数が減ったり増えたりしても,質量に関しては影響が無視できるのです。
よって,電荷については考える必要がなく,イオンを構成する原子について原子量の総和が式量となります。単位はつきません。
例えば,硫酸イオンの式量は,イオン式のSO42-に基づき,32×1+16×4=96です(S=32,O=16)。
スポンサーリンク